细胞侵袭实验提供了一个研究细胞侵袭能力的体外系统。具体应用包括评估肿瘤细胞的转移潜能,细胞外基质成分或抗肿瘤药物抑制转移的作用,转移细胞中细胞表面蛋白或基质金属蛋白酶的表达改变;正常细胞如胚胎干细胞、细胞滋养细胞、内皮细胞和成纤维细胞的侵袭能力。
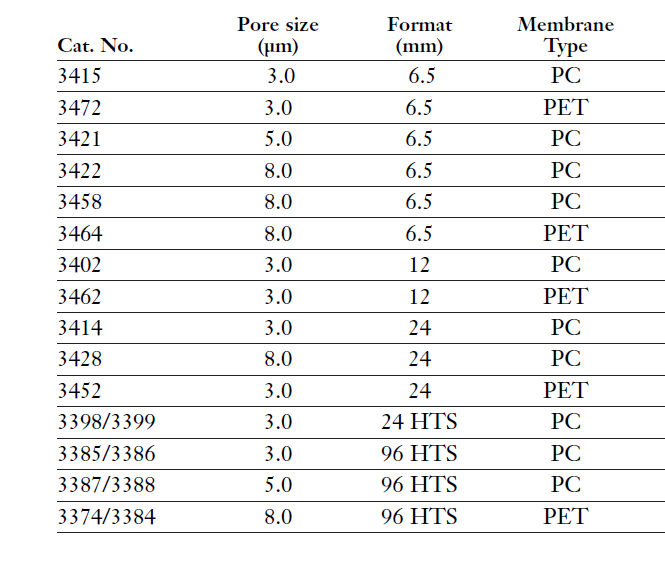
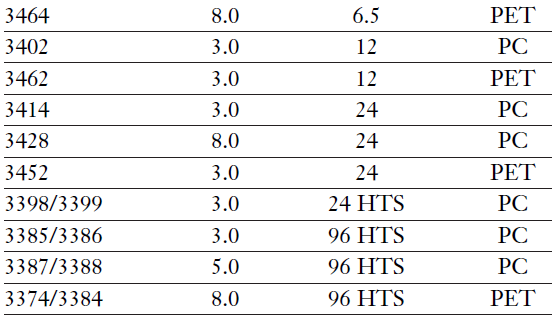
包被康宁Matrigel® 的穿透性小室为体外研究细胞的侵袭性提供了一个相对简便的方法。康宁 Matrigel在体外作为重组的基底膜,封闭膜的小孔并阻止非侵袭性细胞穿过膜迁移。侵袭性细胞(恶性和非恶性)分泌蛋白酶,并通过酶促降解康宁Matrigel进而通过膜孔侵入。膜可以通过光学和电子显微镜观察,且在染色后可以很容易地切下。本期小C讲堂,将手把手与大家分享具体的实验步骤。以下操作步骤已针对 HT-1080 人纤维肉瘤细胞在康宁Matrigel 包被的穿透性小室(24孔,8.0 μm 孔径,如康宁货号3422或3464)上进行了优化。结果可能因实验条件而异,包括细胞、培养基、孵育时间、细胞接种密度和化学诱导物(趋化因子或血清等)。因此,应针对每个具体实验系统进行优化,包括Transwell孔径的正确选择。
1.1 将Matrigel埋在冰盒里,置于 4°C 冰箱中过夜融化。融化后,旋转瓶身以确保Matrigel均匀分散。将Matrigel在冰上使用无菌技术进行分装等操作。
注意:让包被缓冲液在冷室或冰箱的冰浴中冷却两个小时。 任何与 Matrigel接触的吸头、注射器或容器在使用前都必须预冷。
1.2 制备包被液:将 Matrigel 与包被缓冲液混合(最终浓度为200 至 300 μg/mL),通过轻轻旋转彻底混合含有 Matrigel 的包被液。
注意: 您可根据您的细胞种类、侵袭能力等优化Matrigel 包被浓度,并通过预实验进行验证。
1.3 使用无菌注射器或移液器小心地将 0.1 mL Matrigel 包被液添加到每个小室。 尽量减少 Matrigel 与小室侧壁的接触。
1.4 在 37°C 下孵育包被的小室2小时。 在使用前小心地除去小室中剩余的液体(包被缓冲液),请勿触碰小室底部,以免破坏膜上包被好的Matrigel。包被好的小室即可接种细胞了。推荐您在包被的当天使用包被好的小室。
2.0 侵袭步骤
2.1 准备相同数量的对照(未包被)小室。
2.2 为侵袭实验准备细胞,根据您的要求培养细胞(例如,培养基、血清浓度、汇合度)。对于 HT-1080,我们建议培养至约 70% 至 80% 的汇合度,然后再接种至小室中。
2.3 准备适量的细胞,用于 24 孔板的小室。在每个 24 孔小室中加入相应的细胞悬液。
注意:要确定您的细胞类型在小室生长表面的最佳接种密度,请依据在普通培养器皿上的正常接种密度设定区间(细胞数/cm2)。 例如,如果您当前以 1 x 105 个细胞/cm2接种密度培养,则可大约在 5 x 104 到 5 x 105 个细胞/cm2之间确定最佳接种密度。
2.4 在孔板中加入培养基(含化学诱导物,如趋化因子或血清),同时设置无化学诱导物的对照组。
注意:确保在小室下方没有气泡。
2.5 在 37°C、5% CO2 的培养箱中培养12-24 h(孵育时间需要通过预实验优化以确定)。
3.0 检测
3.1去除未侵袭的细胞
去除孔板和小室中的培养基。将用培养基蘸湿的棉签伸入小室的上部,以平缓但稳定的力度按压,同时轻柔擦拭整个区域。另取一支棉签,用培养基润湿后重复上述步骤。
3.2细胞染色
注意:细胞染色可选择不同的方法,包括Diff-Quik试剂盒染色,H&E染色,结晶紫染色或1% 甲苯胺蓝染色。具体染色方法可参考选用的染色试剂说明书。
3.3计数侵袭细胞
注意:通过显微镜对附着在小室膜下侧的细胞进行图像采集,用于细胞计数。也可以直接镜下计数细胞。
注意:计数细胞时, Transwell膜中心的视野和膜边缘的视野都需要选择,以便准确体现示穿过整个膜的细胞数。
确定侵袭细胞百分比有两种方式。
第一种方式:
A.计数随机选取的小室视野中的细胞总数并取平均值(每孔请至少选取5个视野进行计数)。
示例:203、210、220、206 和 213,平均值 = 210
B.将此数字除以显微镜视野的面积,然后将其乘以Transwell 小室的膜面积。
示例:(210 / 0.001 cm2) x 0.33 cm2 = 69,300 个细胞
C.侵袭百分比可以通过将侵袭的细胞数除以接种的细胞数来计算。
第二种方式:

示例:(69,300/100,000) x 100% = 69.3%

文章来源于康宁生命科学








